Artículo
11 feb 2026
Guía completa del participante en estudios clínicos de bioequivalencia
Entienda cómo funcionan los estudios clínicos de bioequivalencia, quién puede participar, cuáles son los beneficios y cómo inscribirse de manera segura en Synvia.

Los estudios clínicos de bioequivalencia forman parte de una etapa importantísima para garantizar que los medicamentos genéricos lleguen al mercado con la misma seguridad, calidad y efectividad del medicamento de referencia (originales).
Estos estudios permiten que millones de personas tengan acceso a tratamientos confiables a precios más accesibles — y la participación de voluntarios saludables es lo que hace todo esto posible.
Synvia es líder en investigaciones clínicas en América Latina, con un equipo formado por más de 800 profesionales y uno de los mayores parques analíticos del continente.
Durante 20 años de actividad, hemos hecho muchas contribuciones a la efectividad y mejora de los medicamentos disponibles en las farmacias de cada rincón de Brasil:
+1.800 estudios realizados +30.000 participantes 15 mil m² de infraestructura |
Estos números muestran la escala, la responsabilidad y la seriedad que involucran cada estudio llevado a cabo por la empresa. ¿Quieres entender más sobre el tema? ¡Continúa leyendo!
¿Cómo funcionan los estudios clínicos de bioequivalencia?
Los estudios clínicos de bioequivalencia se realizan con personas saludables para comparar la velocidad y la cantidad con que el medicamento genérico y el medicamento de referencia (original) son absorbidos por el organismo.
Es a través de estas pruebas que se demuestra que ambos medicamentos se comportan de la misma manera en el cuerpo, garantizando que el genérico sea tan seguro y calificado como el original.
Estos estudios clínicos también ofrecen a los participantes la oportunidad de contribuir directamente a la salud pública y, además, recibir una compensación financiera por su tiempo y colaboración.
¿Quieres ayudar a validar medicamentos genéricos y recibir una compensación por tu contribución? Haz clic aquí.

¿Quién puede participar en las investigaciones de bioequivalencia?
Pueden participar en los estudios clínicos de bioequivalencia personas saludables, mayores de edad y que cumplan con los criterios definidos para cada protocolo. Los principales requisitos incluyen:
Ser mayor de 18 años. | Tener buenas condiciones físicas. | No hacer uso de medicamentos continuos, salvo aprobación médica. |
No tener antecedentes de enfermedades graves. | No estar embarazada ni amamantando (en el caso de mujeres). | Estar dispuesto a cumplir con el ayuno, recolecciones y horarios establecidos. |
La confirmación de esta elegibilidad se realiza durante la selección clínica, etapa que garantiza seguridad para todos los involucrados.
Haz clic aquí y sé uno de los primeros en ser llamado para nuevos estudios de bioequivalencia.
Antes del estudio de bioequivalencia: ¿cómo prepararse?
Antes de participar en los estudios clínicos de bioequivalencia, es importante entender que algunas etapas de preparación garantizan tu seguridad y la calidad de los resultados.
A continuación, encontrarás exactamente qué hacer antes de este momento y cómo prepararte para que todo transcurra de la mejor manera posible. ¿Vamos?
Preparación para la selección
La preparación para la selección es simple, pero fundamental para garantizar que tus exámenes reflejen con precisión tu estado de salud. Pequeños cuidados en los días previos ayudan a evitar alteraciones en los resultados y aumentan tus posibilidades de ser aprobado para participar en el estudio.
Antes de avanzar a la etapa de evaluación, revisa las orientaciones a continuación y asegúrate de que todo esté de acuerdo, para que el estudio continúe sin dificultades:
Llevar un documento oficial con foto: DNI o licencia de conducir.
Dormir bien la noche anterior: esto ayuda en los resultados de los exámenes.
Evitar bebidas alcohólicas por al menos 48h antes de la selección.
Evitar actividad física intensa: puede alterar parámetros clínicos.
Ayunar si se solicita: según indicaciones del equipo.
Informar sobre cualquier problema de salud reciente: la transparencia es esencial.
¿Qué sucede en la selección clínica?
Durante la selección clínica, algunos profesionales de la salud realizan evaluaciones completas para garantizar que el participante esté perfectamente apto para el avance de los estudios clínicos.
Evaluación médica: conversación sobre salud, hábitos e historial.
Exámenes de laboratorio: sangre y orina para verificar parámetros generales.
Signos vitales: presión arterial, temperatura, frecuencia cardíaca.
Electrocardiograma (cuando sea necesario): evaluación de la actividad cardíaca.
Firma del Consentimiento Informado (CI): documento que explica derechos y deberes del participante.
La selección no garantiza la participación — solo confirma si la persona cumple con los criterios necesarios. Regístrate ahora y recibe la invitación tan pronto como se abran las plazas:
Etapas durante el estudio: ¿cómo funciona cada una?
Antes de detallar cada etapa, es importante entender que todos los estudios clínicos de bioequivalencia siguen protocolos rigurosos, aprobados por Comités de Ética, y cuentan con un seguimiento constante por equipos entrenados.

¿Quieres participar en la investigación de bioequivalencia de Synvia? Haz clic aquí para acceder a nuestro Whatsapp y realizar tu inscripción.
Reglas y beneficios de los estudios clínicos de bioequivalencia
Los estudios clínicos de bioequivalencia siguen normas rigurosas para proteger al participante y garantizar que todos los resultados obtenidos sean realmente fiables.
Estas reglas existen para estandarizar cada etapa del estudio, mantener la seguridad de todos y asegurar que los datos obtenidos representen con precisión el comportamiento del medicamento en el organismo.
Antes de participar, es importante conocer estas orientaciones. A continuación, encontrarás las principales.
Las reglas de los estudios clínicos de bioequivalencia
HACER | NO HACER |
✅ Cumplir con los horarios de ayuno y alimentación. ✅ Informar inmediatamente sobre cualquier malestar. ✅ Llevar los documentos solicitados. ✅ Seguir las orientaciones del equipo. | ❌ No consumir alcohol antes o durante el estudio. ❌ No practicar ejercicios intensos en los días anteriores. ❌ No ocultar información médica. ❌ No tomar medicamentos sin informar al equipo. |
Beneficios de participar en los estudios de bioequivalencia
Participar en estudios clínicos de bioequivalencia es más que contribuir al desarrollo de medicamentos genéricos seguros y efectivos.
El participante también recibe beneficios directos que hacen que la experiencia sea positiva, estructurada y gratificante:
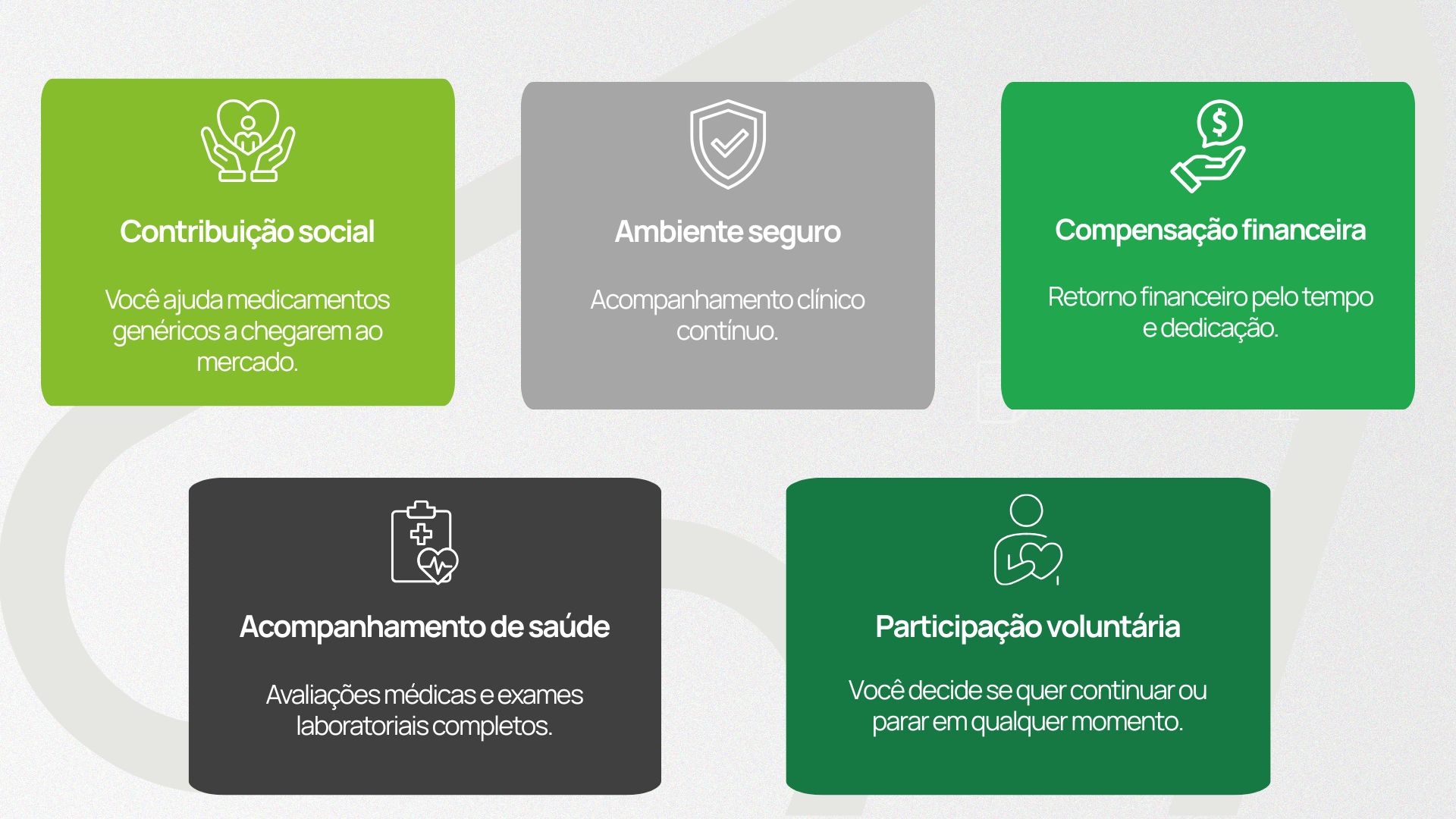
Ética, seguridad y transparencia
La base de cualquier estudio clínico es la ética, y esto es especialmente cierto en los estudios de bioequivalencia realizados por Synvia.
Todo el proceso está estructurado para proteger al participante, ofrecer total transparencia y garantizar que cada etapa sea supervisada por profesionales calificados.
Antes de comenzar, el participante recibe toda la información necesaria para decidir si desea participar y tiene la garantía de que puede desistir en cualquier momento — sin justificación y sin perjuicio.
Aprobados por el Comité de Ética en Investigación (CEP).
Seguimiento constante por médicos, enfermeras y equipo técnico.
Explicación completa en el CI antes de cualquier procedimiento.
Derecho a desistir en cualquier momento, sin justificación.
¿Cómo participar en el próximo estudio?
Participar en los próximos estudios clínicos de bioequivalencia es simple y completamente guiado por el equipo de Synvia. Solo necesitas llenar tu inscripción haciendo clic aquí y esperar el contacto para la selección.
Tan pronto como se abran nuevas plazas, los inscritos serán llamados en orden de disponibilidad — por eso, cuanto antes te inscribas, mayor será la posibilidad de participar en el próximo ciclo.
Si deseas formar parte de los próximos estudios, ayudar directamente en la liberación de medicamentos más accesibles y ser recompensado por ello, solo necesitas realizar tu inscripción y seguir las próximas etapas.
Tu participación es voluntaria, totalmente segura y de extrema importancia para que investigaciones relevantes continúen ocurriendo en Brasil.
¿QUIERES PARTICIPAR EN EL PRÓXIMO ESTUDIO? Haz clic aquí, inscríbete ahora y recibe prioridad en las próximas plazas. |
Preguntas frecuentes de los participantes en investigaciones de bioequivalencia
1. ¿Qué es exactamente un estudio de bioequivalencia? |
Un estudio de bioequivalencia compara un medicamento genérico con su versión de referencia para verificar si ambos tienen el mismo comportamiento en el organismo — es decir, si la absorción, distribución y eliminación del principio activo ocurren de forma equivalente. Esto asegura que el genérico tendrá eficacia y seguridad similares a la original. |
2. ¿Quién puede participar en estos estudios? |
Pueden participar personas saludables. Debes seguir los prerequisitos a continuación:
|
3. ¿Cómo me inscribo y soy seleccionado? |
Comienzas con una inscripción — luego viene una pre-selección digital para evaluar la elegibilidad. Si el perfil está de acuerdo, se agendará un chequeo completo (exámenes de laboratorio, cardiológicos, etc.). Con exámenes dentro de los parámetros, serás convocado para participar en el estudio. |
4. ¿Necesito ser internado? ¿Cuánto dura la participación? |
Depende del protocolo del estudio. Algunos exigen internación para recolecciones, monitoreo y administración del medicamento; otros pueden tener parte ambulatorial. El tiempo varía según el diseño del estudio, pero toda la logística (internación, exámenes, alimentación, descanso) es detallada por el equipo de Synvia. |
5. ¿Los estudios son seguros? ¿Hay riesgo para el participante? |
Sí — la seguridad es prioridad: todos los protocolos son revisados y aprobados por el Comité de Ética en Investigación (CEP), y siguen normas nacionales e internacionales (incluyendo regulación de ANVISA). Los participantes firman el Consentimiento Informado (CI) antes de cualquier procedimiento, reciben información clara sobre riesgos y pueden desistir en cualquier momento. |
6. ¿Qué ofrece Synvia a los participantes como beneficio? |
Los participantes tienen acceso a exámenes y monitoreo médico gratuitos, seguimiento de salud, alimentación, estructura cómoda durante el estudio y compensación financiera por la participación — como retribución por el tiempo invertido y colaboración con la investigación. |
7. ¿Y si necesito desistir? ¿Puedo salir en cualquier momento? |
Sí. La participación es voluntaria, y el voluntario puede desistir en cualquier momento, sin necesidad de justificar y sin perjuicio. Este derecho está garantizado por la ética de la investigación y expresado en el CI. |
8. ¿Los datos de salud y personales están protegidos? |
Sí — Synvia sigue normas éticas y regulatorias que garantizan privacidad y confidencialidad de los datos de los participantes. La información personal y de salud se maneja con confidencialidad según la legislación aplicable. |
9. ¿Por qué son importantes estos estudios para Brasil? |
Sin los estudios de bioequivalencia, los genéricos no podrían ser aprobados con seguridad. Garantizan que los medicamentos genéricos tengan la misma eficacia y seguridad que los de referencia — lo que hace que los tratamientos sean más accesibles y democratiza el acceso a la salud en el país. Synvia, con su estructura, contribuye directamente a este proceso. |
10. ¿Cómo sé cuándo hay plazas para participar en un nuevo estudio? |
La inscripción comienza con una inscripción (normalmente a través del sitio o formulario indicado por Synvia). Después de la inscripción, entras en una base de datos de voluntarios. Cuando surja un nuevo protocolo compatible con tu perfil, el equipo se pondrá en contacto para iniciar la selección. |