Biossimilares: O salto estratégico em pesquisa clínica e acesso a terapias biológicas

Nas últimas duas décadas, os medicamentos biológicos transformaram o tratamento de doenças crônicas e complexas, como câncer, artrite reumatoide e diabetes. No entanto, o alto custo dessas terapias tem limitado o acesso de milhões de pacientes em todo o mundo, pressionando sistemas públicos e privados de saúde. Nesse contexto, os biossimilares – medicamentos […]
Disfunção erétil: o que é, causas e tratamentos avançados

PT EN ES Fale Conosco PT EN ES Fale Conosco Blog Synvia Novidades, tendências e insights especializados para você. Receba conteúdo e novidades com prioridade. A disfunção erétil é uma condição que afeta milhões de homens em todo o mundo e, segundo as principais diretrizes médicas, é definida como a incapacidade de alcançar ou manter […]
Imunodeficiência primária: o que é, sintomas e tratamentos
A imunodeficiência primária é uma condição rara, mas que merece cada vez mais atenção. Ela acontece quando o sistema imunológico – a defesa natural do organismo contra vírus, bactérias e fungos – apresenta falhas desde o nascimento. Essas falhas tornam o corpo mais vulnerável a infecções, inflamações e doenças autoimunes. Embora os sintomas possam […]
Fissura Perianal: O que é, sintomas e tratamento

A fissura perianal é uma das causas mais comuns de dor anal persistente, afetando significativamente a qualidade de vida e o bem-estar. Embora muitas pessoas hesitem em procurar ajuda médica por vergonha ou constrangimento, trata-se de uma condição que exige atenção clínica cuidadosa. É estimado que até 20% dos pacientes que procuram atendimento […]
Esquizofrenia: Sintomas, Diagnóstico, Cuidados e Avanços Científicos

A esquizofrenia é uma condição de saúde mental que afeta milhões de pessoas no mundo, alterando o modo como pensam, percebem a realidade, expressam emoções e se relacionam. Para muitos, o diagnóstico traz consigo dúvidas, medos, isolamento. Mas também há espaço para esperança: com acompanhamento médico especializado, suporte terapêutico e uma rede de apoio […]
Cólica menstrual intensa é normal? Quais os tratamentos?

A cólica menstrual intensa é um sintoma comum, mas nem sempre “normal”. Em muitos casos, pode indicar algo além do que simplesmente “dor de menstruação”. Estima-se que entre 50% a 90% das mulheres em idade reprodutiva já tenham sentido dor menstrual em algum momento de suas vidas. Em um estudo realizado com universitárias, a […]
Uma nova possibilidade de tratamento para Diabetes Tipo 2
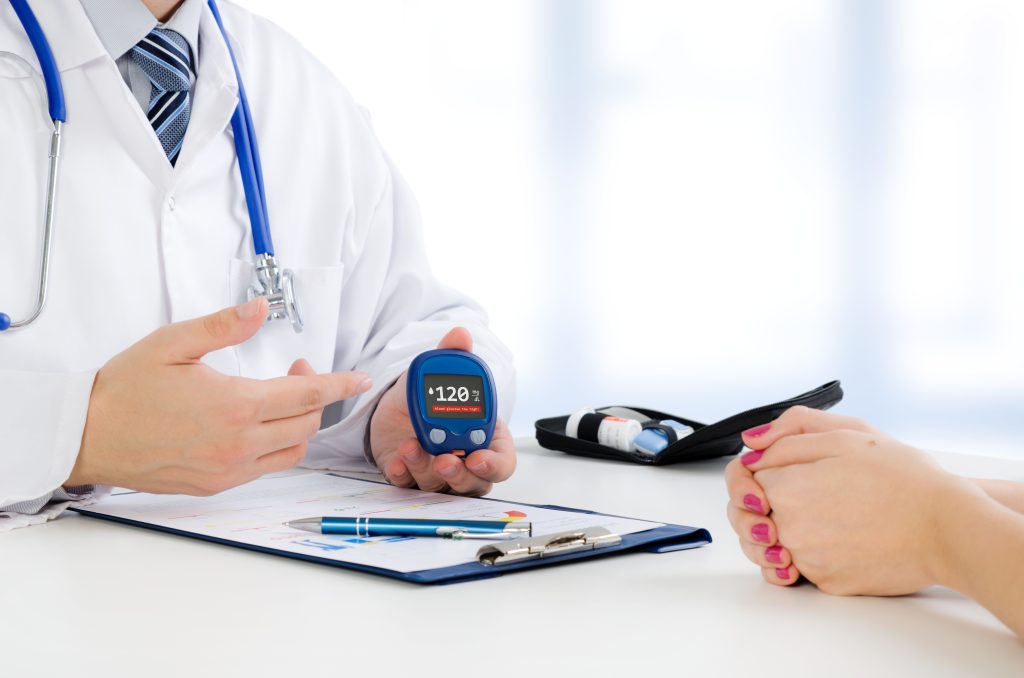
Você convive com diabetes tipo 2? Hoje, milhões de pessoas em todo o mundo enfrentam os desafios diários do diabetes. Só em 2024, a doença foi responsável por 3,4 milhões de mortes – uma a cada nove segundos. Apesar dos avanços da medicina, ainda não existe cura definitiva. Mas há um caminho que pode transformar […]
Gerenciamento de Projetos na Indústria Farmacêutica: Como Elevar a Eficiência dos Estudos Clínicos

O caminho entre o desenvolvimento de um medicamento e sua chegada ao mercado engloba múltiplos desafios que envolvem desde a coordenação de equipes especializadas até o cumprimento de prazos rígidos e normas internacionais. É nesse cenário que a gestão de projetos na indústria farmacêutica se torna um diferencial decisivo. Além dos cronogramas, é preciso conduzir processos […]
Estudos Clínicos na América Latina: Alinhamento Regulatório e Potencial de Mercado
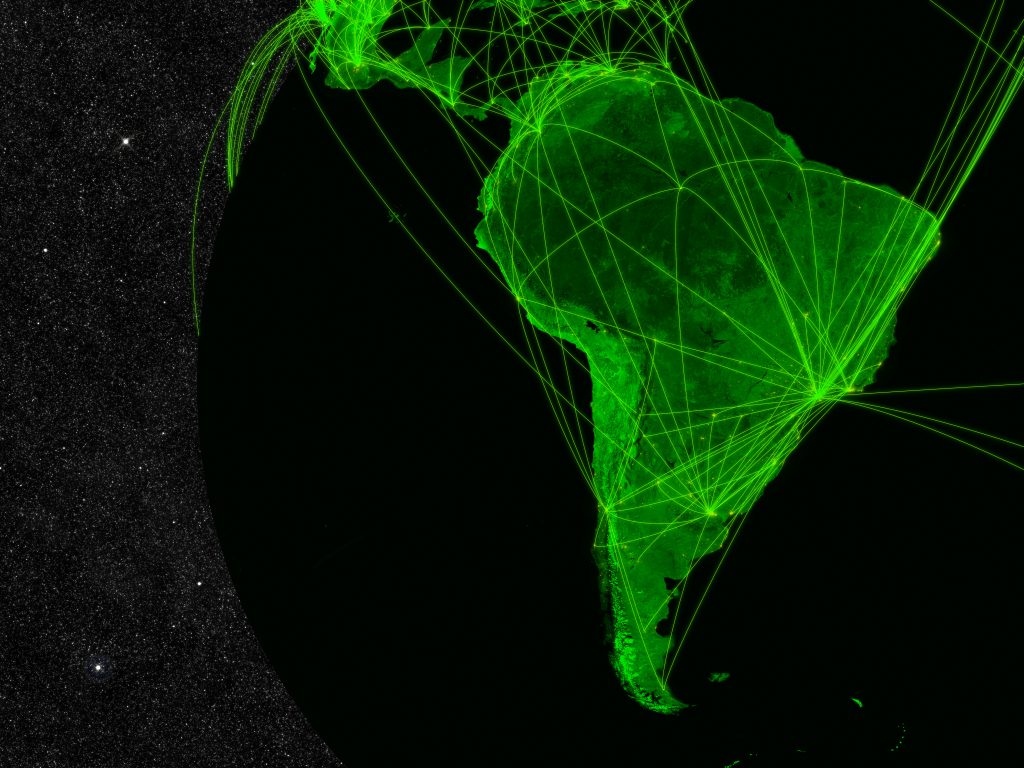
A América Latina (LATAM) vem ganhando força rapidamente como uma região estratégica para o desenvolvimento global de estudos clínicos. Com melhorias nos sistemas regulatórios e maior alinhamento com padrões internacionais, a região se consolida como destino-chave para patrocinadores que buscam acelerar cronogramas mantendo padrões éticos e sem comprometer a qualidade dos dados. Para as […]
8º Relatório Anual de Pesquisa Clínica da ANVISA 2024: As principais conclusões

Resumimos os principais pontos de destaque do 8º Relatório Anual de Pesquisa Clínica de Medicamentos e Produtos Biológicos da ANVISA, referente ao ano de 2024, explicando o cenário que ele desenha para a indústria farmacêutica nacional. O 8º Relatório de Pesquisa Clínica ANVISA, publicado no final de junho de 2025, traz dados abrangentes […]
